Термини „анода“ и „катода“ представљају кључне појмове у електрохемији и електричним колима. Ове две врсте електрода имају виталну улогу у различитим системима, од једноставних батерија до напредних технологија.
У наставку ћемо детаљно истражити њихове разлике, као и позитивне и негативне ознаке, те како лако препознати која је позитивна, а која негативна.
Шта је електрода?
Пре него што се упустимо у детаље о томе шта представљају катода и анода, неопходно је разумети основни концепт електроде. У суштини, електрода је материјал који омогућава провођење електричне енергије, омогућавајући електричној струји да уђе или изађе из неметалног окружења, попут електролитске ћелије.
Једноставно речено, електрода служи као проводник који успоставља електрични контакт са неметалним делом кола.
Шта је анода?

Поларитет електроде, било да је реч о аноди или катоди, зависи од типа кола. Анода је електрода на којој се одвија процес оксидације, што резултира губитком електрона. У галванској ћелији (која претвара хемијску енергију у електричну, као што је то случај приликом пражњења батерије), анода функционише као негативна електрода. Разлог томе је што, током оксидације, електрони остају на електроди и крећу се кроз спољно коло.
Насупрот томе, у електролизи, где електрична струја покреће проток електрона у супротном смеру, анода постаје позитивна електрода.
Шта је катода?
 Кредит за слику: Распберри Пи
Кредит за слику: Распберри Пи
Катода је место где се одвија редукција, што подразумева прихватање електрона. У галванској ћелији, катода се понаша као позитивна електрода јер јони подлежу редукцији прихватајући електроне са електроде, након чега се издвајају.
Са друге стране, у електролизи, катода је негативни терминал који привлачи позитивне јоне из раствора.
Анода против катоде: разјашњавање поларитета
У почетку се веровало да струја тече од позитивног ка негативном пола, што је у супротности са оним што данас сматрамо истинитим. Ова рана заблуда је навела неке да повезују аноду са негативношћу, а катоду са позитивношћу.
Међутим, уз правилно разумевање улога оксидације и редукције на свакој електроди, лако се може идентификовати која је анода, а која катода – при чему је одлучујући фактор тип кола.
Шта је електролит у батерији?
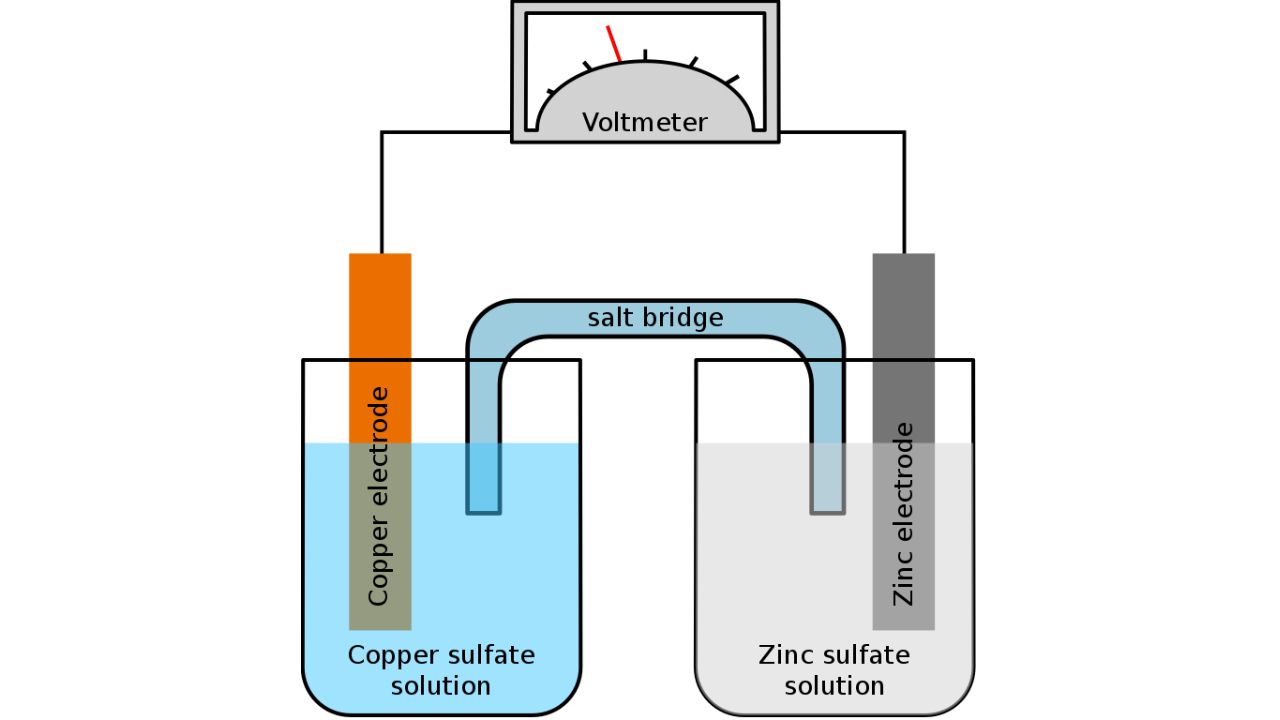 Кредит за слику: Тинук/грингер/Викимедиа Цоммонс
Кредит за слику: Тинук/грингер/Викимедиа Цоммонс
У батеријама, електролит је медијум који омогућава проток јона између аноде и катоде, док их истовремено одржава електрично неутралним. Ово кретање јона је неопходно за хемијске реакције које се одвијају током процеса пуњења и пражњења. За више информација о овоме, прочитајте како функционишу литијум-јонске батерије.
Који је позитиван?
Да би се разумео поларитет када је реч о електродама у ћелији или колу, важно је узети у обзир две реакције које се одвијају на два различита места. У галванској ћелији, анода подлеже оксидацији и функционише као негативна електрода, док у електролизи постаје позитивна. Насупрот томе, катода олакшава редукцију и функционише као позитивна електрода у галванској ћелији, али делује као негативни терминал у електролизи.